一、项目实施情况:
一、项目实施情况(请就研究目标、研究过程、研究成果、研究心得作全面总结,3000字以内):
(一)研究目的
解决纳他霉素合成与菌丝分化的关联调控机制,为纳他霉素的高效发酵生产及高产菌株的构建提供全新的理论依据。
(二)研究过程
1. 明确MI-MII分化过渡期ROS对激活纳他霉素生物合成的浓度阈值
(1)分析褐黄孢链霉菌MI-MII分化过渡期ROS的变化及纳他霉素合成:分别在发酵前期取样,HPLC测定纳他霉素产量,同时检测ROS浓度与菌丝分化状态,分析MI-PCD-MII分化时期与ROS关系。(已部分完成)。
(2) MI-MII分化过渡期ROS激活纳他霉素生物合成的阈值:分别在发酵前期(48h前)不同时间点,利用H2O2和NAC建立不同浓度ROS组,分析ROS对纳他霉素产量以及产生时间的影响。
(3) ROS阈值对纳他霉素生物合成基因表达的激活:依据ROS浓度阈值,胞内浓度达到激活纳他霉素合成阈值及以上时,RT-qPCR分析纳他霉素合成基因簇相关基因转录的激活作用。
2.解析褐黄孢链霉菌中ROS对OxyR的激活作用机制
(1) 分析ROS体外及体内条件下对OxyR的氧化激活作用:构建OxyR-His重组蛋白,硫醇荧光Elisa试剂盒定量分析ROS对OxyRred的氧化作用。构建oxyR基因缺失菌株F607-ΔoxyR及OxyR FLAG重组质粒pMS82-FLAGH,FLAG抗体Western blot分析验证OxyR的氧化程度,明确在褐黄孢链霉菌体内ROS氧化OxyRred为OxyRox阈值。
(2) OxyR的Cys残基突变对氧化还原能力和纳他霉素产生的影响:利用软件预测 OxyR蛋白的结构域中的保守序列。体外氧化还原实验阐明不同结构域突变体对接收ROS 信号并发生氧化水平的影响。
3.解析MI-MII分化过渡期OxyR激活纳他霉素合成的关系并构建高产菌株
(1)验证OxyRox对纳他霉素的激活作用:依据ROS激活纳他霉素生物合成的阈值;巯基活性保护剂AMS捕获后,Western blot分析验证OxyR的氧化程度;
(2)RT-qPCR分析sgnM、sgnR和其他靶基因表达量。
(3)构建基于纳他霉素外排的工程菌,验证OxyR和ROS对纳他霉素生物合成的影响。
(二)技术路线
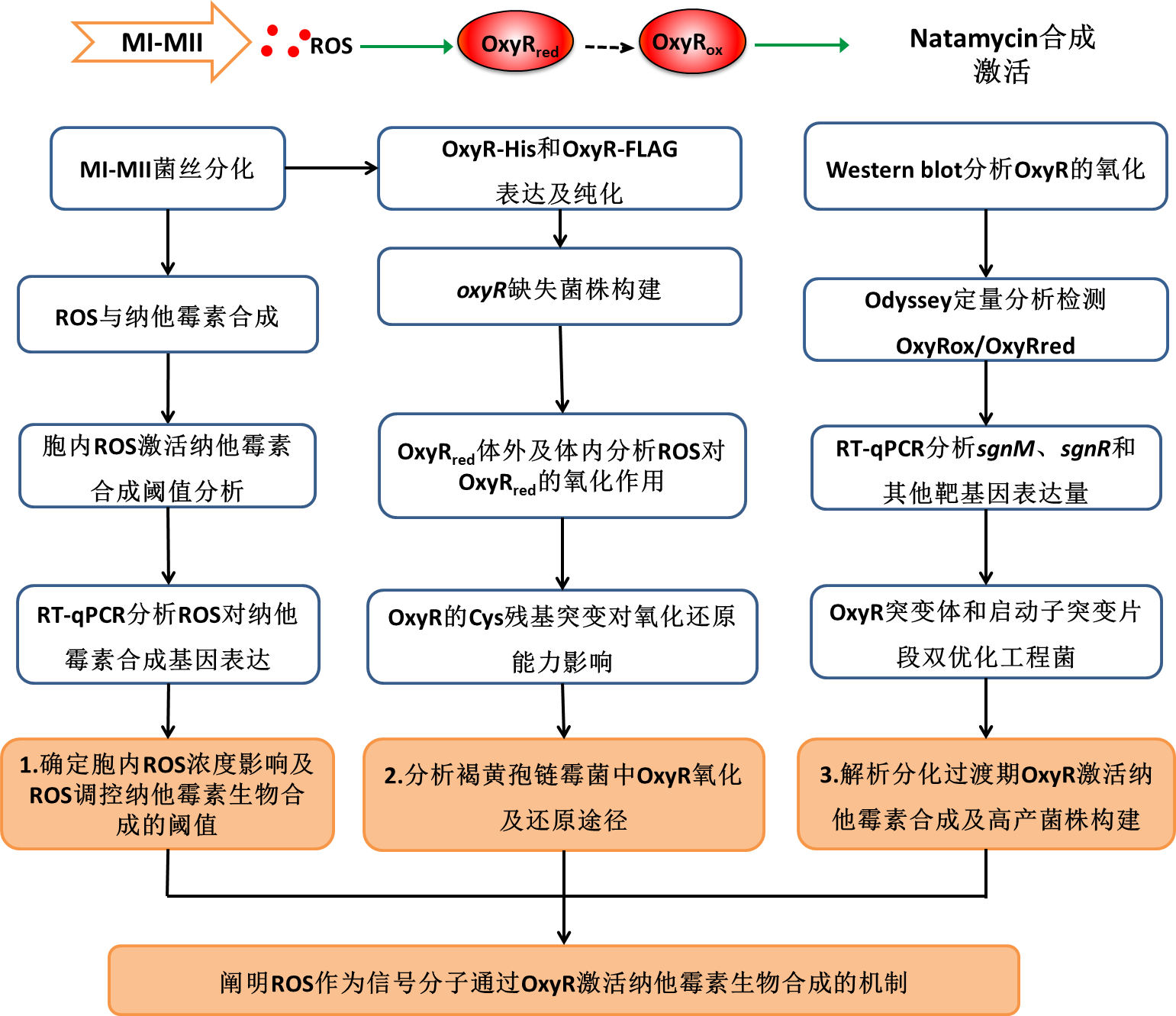
(三)试验方案实施情况
1. MI-MII分化过渡期ROS积累激活纳他霉素生物合成
分别在发酵不同时间点(前MI、MI-MII过渡期和MII后期)测定胞内ROS和纳他霉素产量,结果表明纳他霉素在MI-MII过渡期开始生物合成,且ROS的快速积累期(36-48h)是纳他霉素对数合成期的初始阶段(图1 A、B)。我们进一步分析发现,纳他霉素合成基因簇内的sgnE基因表达产生的SgnE蛋白具有胆固醇氧化酶活性,其酶促反应终产物之一为H2O2,因此,我们构建了sgnE敲除菌株,发现sgnE缺失后,纳他霉素生物合成被阻断,而回补该基因后,纳他霉素生物合成得到恢复,如图2 C。同时,伴随纳他霉素生物合成的阻断,胞内H2O2的浓度在纳他霉素合成期(36 h-120h)显著下降至1.41-2.83 μmol/g 湿菌体,F607则达到5.62-19.8 μmol/g湿菌体,回补该基因后,胞内H2O2的浓度则恢复至5.17-19.65μmol/g。分析纳他霉素生物合成和H2O2代谢关系发现,当胞内2O2浓度过低(~小于5 μmol/g) 时,纳他霉素的生物合成是抑制状态;而当浓度过大(~超过20 μmol/g)时,纳他霉素生物合成速率同样下降;在5-20 μmol/g的胞内H2O2浓度下,纳他霉素生物合成激活,因此初步确定5-20 μmol/g的胞内H2O2浓度是影响纳他霉素生物合成的阈值范围。

图1 褐黄孢链霉菌MI-MII菌丝发育及ROS与纳他霉素合成的关系
(A)F607菌株胞内H2O2和纳他霉素关系;(B)F607菌株MI和MII菌丝分化状态;(C)sgnE 敲除及回补菌株构建策略;(D) sgnE 敲除及回补菌株PCR验证;(E and F) sgnE 敲除及回补菌株 胞内H2O2 and 纳他霉素产量测定. F607, 对照; DE13, sgnE 敲除菌株; CE13, sgnE 回补菌株。
2. SgnE催化产生H2O2的关键位点的生物信息学分析
为进一步明确H2O2的信号分子作用,在敲除菌株DE13发酵60g时,添加了100 μM H2O2,发现胞内H2O2浓度迅速增加到11.25 μmol/g (60.5 h),在66 h 则检测到了纳他霉素的产生 (0.08 mg/L),图2A。因此,信号分子对纳他霉素生物合成具有重要作用,构建
有利于信号分子产生的SgnE对纳他霉素产量的提升及高产菌株的构建具有指导意义,本项目对H2O2信号分子的产生进行了进一步的生物信息学分析。
通过同源建模构建SgnE的空间结构模型(图2 C),并依此对SgnE反应底物-胆固醇、豆甾醇和麦角甾醇进行了分子对接分析(图2 D)。分析发现,褐黄孢链霉菌来源的SgnE的酶促活性中心被包裹在酶分子中间,行成疏水性结构比较强的反应活性口袋,这种结构的行成有利于非水溶性底物与酶分子的催化反应。外源表达纯化SgnE蛋白(图2 E)并分析酶活(图2 F)发现,SgnE能够催化发酵培养基中的麦角甾醇和豆甾醇产生H2O2,表明在纳他霉素发酵过程中,ROS重要来源是SgnE的酶促反应,该反应的底物是发酵培养基中的麦角甾醇和豆甾醇。

图2 SgnE催化产生H2O2的底物分析
(A)H2O2添加恢复纳他霉素合成。F607, 对照; DE13, sgnE 敲除菌株; CE13, sgnE 回补菌株;(B)胆固醇、豆甾醇和麦角甾醇结构式;(C)SgnE 三维模型;(D) SgnE催化活性中心;(E) SgnE外源表达及纯化敲除及回补菌株;(F)SgnE催化不同底物的酶活。
3. 分析褐黄孢链霉菌中ROS与氧化响应蛋白OxyR对纳他霉素合成的影响
OxyR属于LysR蛋白家族,是一种重要的ROS信号感应蛋白,N端具有DNA结合结构域,C端含有底物结合结构域。OxyR在H2O2的作用下形成可逆的二硫键,由还原型非激活态(OxyRred)转化为氧化型激活态(OxyRox),调控相关靶基因转录。本项目构建了OxyR菌株,并研究了OxyR在菌丝分化和纳他霉素生物合成的影响。研究结果显示,ROS信号响应蛋白OxyR编码基因的敲除显著降低了纳他霉素的生物合成(0.53 g/L),为出发
菌株的11.8%;而回补该基因则恢复纳他霉素生物合成能力到3.24 g/L,表明OxyR是纳他霉素生物合成的正调控因子(图3)。
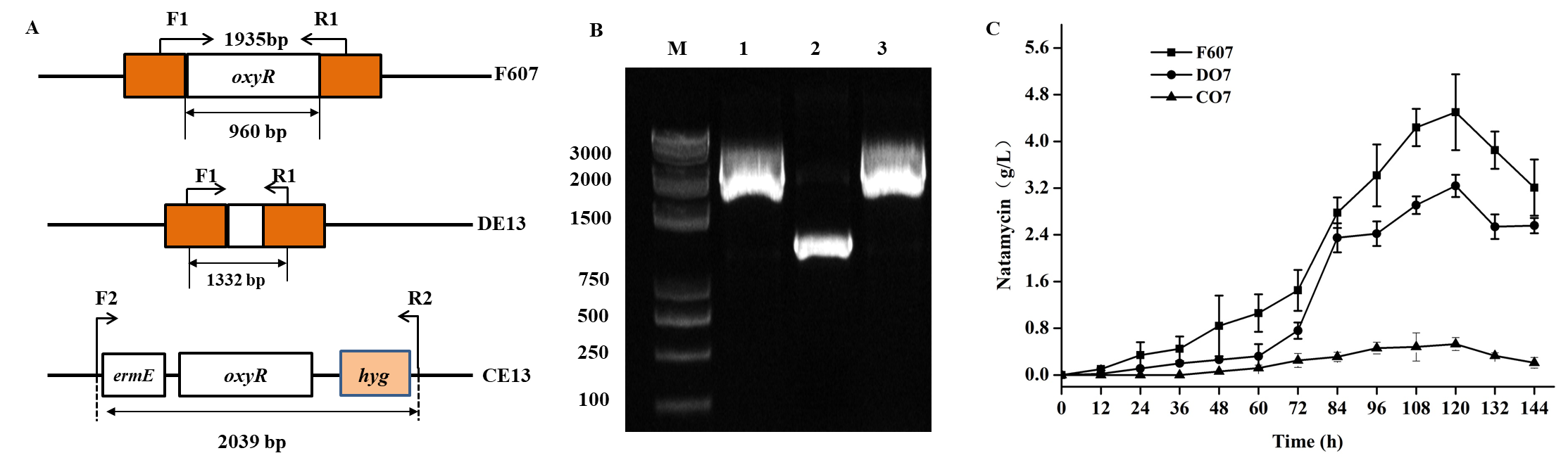
图3 OxyR对纳他霉素生物合成的影响
同时,我们分析了OxyR的缺失对菌丝分化的影响,扫描电镜结果分析发现,OxyR的缺失影响了菌丝的正常分化,使得MI到MII阶段的发育大大延迟,且产孢时间明显滞后;投射电镜进一步分析发现,OxyR缺失菌株中菌丝分化和孢子产生所需的隔膜明显被抑制。因此OxyR在MI-MII菌丝分化过程中也表现为正调控作用(图4)。
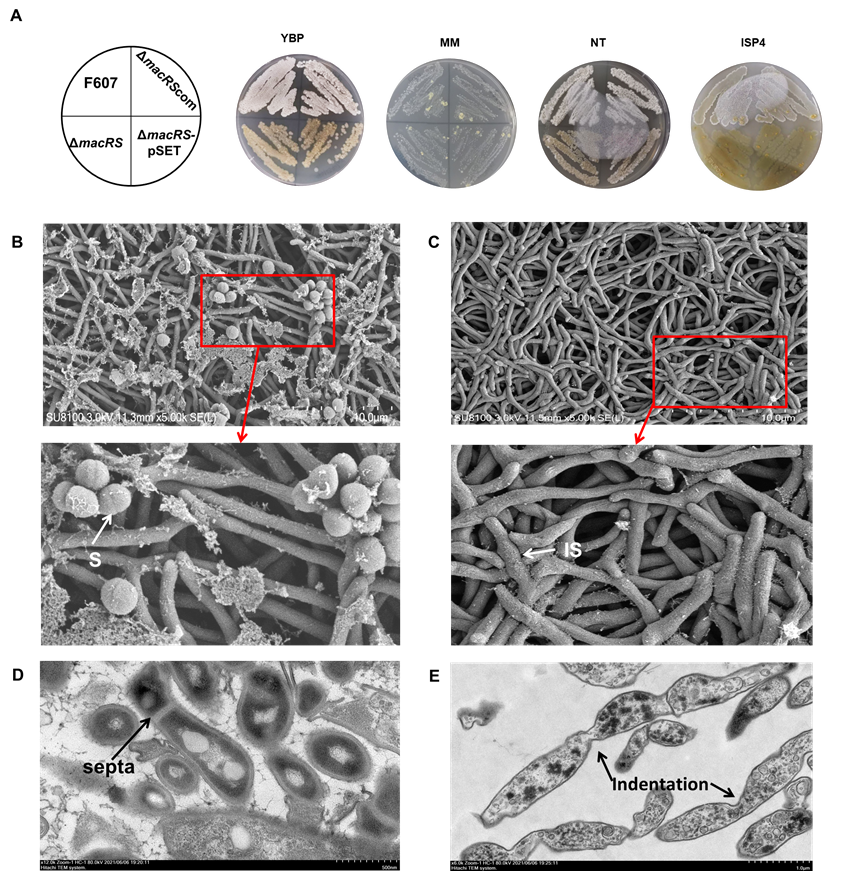
图3 OxyR对褐黄孢链霉菌菌丝分化的影响
4. 解析OxyR响应氧化还原方式
解析OxyR调控纳他霉素合成和菌丝分化靶基因,我们首先通过生物信息学手段筛选了其潜在可能的靶基因,利用SWISS-MEDOL和Discovery Studio 3.0构建的S. gilvosporeus OxyR三维结构模型结果表明,S. gilvosporeus还原态OxyR中Cys212与Cys221中心原子距离为14.896 Å,相比于E.coli中Cys199和 Cys208距离(17 Å)更近,更易于形成分子内二硫键;氧化态OxyR Cys212-Cys221结构域构象发生变化,Cys212与Cys221中心原子距离缩短为4.892 Å(图4A)。
OxyR是细菌调控胞内ROS浓度的重要分子,纳他霉素作为还原性次级代谢产物,其生物合成初步被证实受OxyR调控。OxyR蛋白四聚体(A、B、C、D)同源建模及OxyR-sgnR启动子序列的ZDock分析结果显示,四个OxyR单体的DNA结合结构域形成了类“扳手”结构,DNA分子正好穿过该结构。分子动力学模拟发现,还原态OxyR的“扳手”结构与DNA结合较为疏松;氧化态和过氧化态的DNA结合结构域构象则发生变化,氧化态
OxyR的DNA结合部位收缩(图4B)。
以OxyR还原态作为分子对接受体,以H2O2为配体,CDock分子对接发现,OxyR中Cys212和Cys221是H2O2分子感应位点,且Thr142、Gly216和Ile220、Arg196可能分别同Cys212和Cys221构成OxyR信号识别和氧化的关键氨基酸位点(图4 C、D)。OxyR四聚体结构模型显示,四个OxyR单体信号感应结构域的Cys212相互靠近,13.48-22.28 Å范围内形成“H2O2反应口袋”,而Cys221则被包埋在蛋白内部。分子动力学分析发现Cys212在高浓度H2O2下,优先发生氧化或过氧化(图4 E)。因此,以上结果初步表明H2O2-OxyR信号通路中,OxyR可能以Cys212和Cys221及周边氨基酸位点构成信号感应关键氨基酸位点,感应H2O2信号分子。
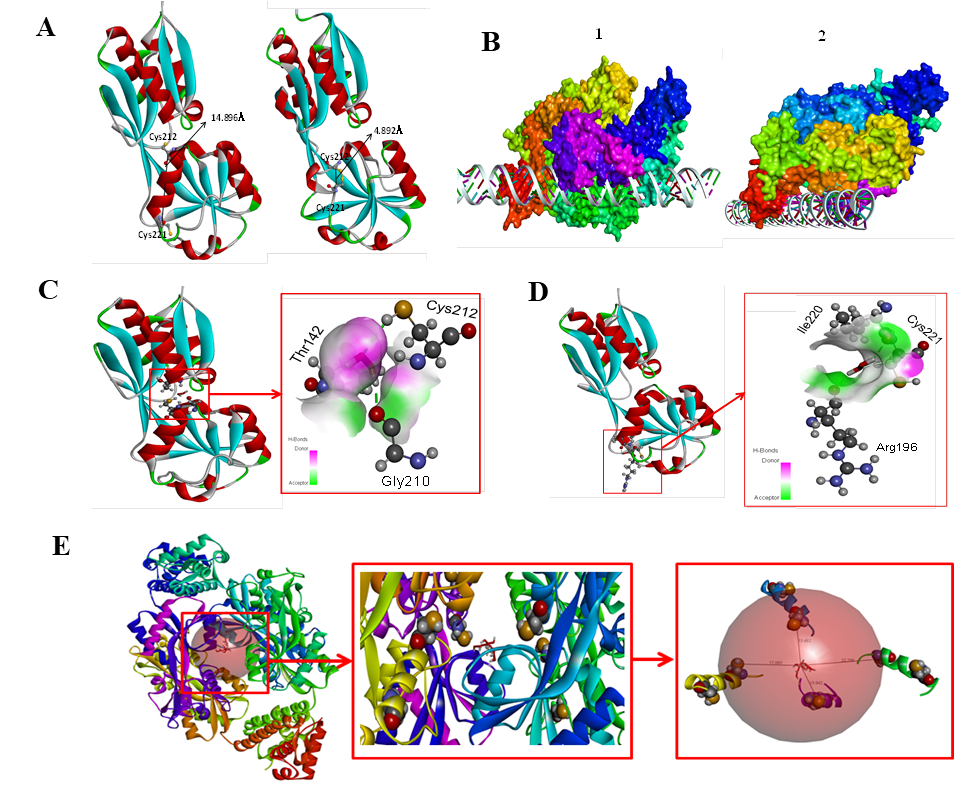
图4 S. gilvosporeus OxyR感应H2O2反应口袋及DNA结合
(A):S. gilvosporeus OxyR单体还原态和氧化态模型, 1:还原态;2:氧化态。(B)OxyR四聚体表面和 “扳手结合结构”。(C-D):OxyR单体的Cys212和Cys221区域同H2O2的CDock分子对接及结合位点。(C):OxyR四聚体Cys212的 “H2O2反应口袋”。
5. 解析OxyR调控纳他霉素合成和菌丝分化的靶基因
前期实验和文献分析发现,OxyR的调控靶点多为氧化应激系统相关基因的表达,在S. avermitilis ATCC31267中OxyR可以调控离子依赖型转录调控因子IdeR的转录,进而调
控链霉菌的发育和次级代谢产物(阿维菌素)的产生。经过对F607中OxyR菌株的转录组测序分析和RT-qPCR验证发现,IdeR同源基因RS24880表达量显著下降,且纳他霉素合成途径特异性调控基因sgnM、sgnR及基因簇合成基因表达量显著下降(图5A、B)。
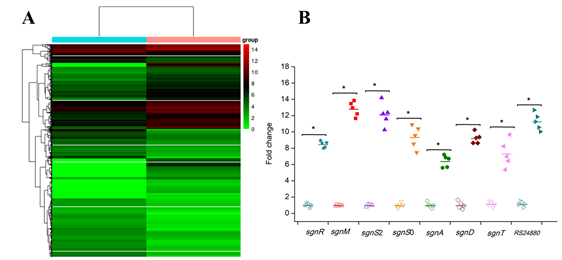
图5 S. gilvosporeus OxyR缺失菌株转录组及相关基因的RT-qPCR验证
(A):S. gilvosporeus OxyR缺失菌株转录组结果, 左:F607;右:OxyR缺失菌株。(B)纳他霉素生物合成及RS24880基因表达量RT-qPCR验证。
进一步利用同源建模和分子模拟技术初步分析了OxyR调控靶基因。分析结果发现OxyR在F607的纳他霉素生物合成途径特异性基因sgnM-sgnR共用启动子片段区域具有结合位点,IdeR同源基因RS24880也具有相似结合位点(GGTCC-15nt-CGGC-15nt-GCCG-9nt-GGACC)(图6)。

图6 OxyR与相关靶基因结合位点的生物信息学分析
(A):S. gilvosporeus 中sgnM-sgnR启动子区OxyR结合位点。(B):sgnM-sgnR启动子序列、RS24880启动子序列与IdeR启动子序列的OxyR结合位点分析。(C):OxyR与靶DNA序列结合的信息学预测。
6. 验证OxyR调控纳他霉素合成和菌丝分化靶基因的结合
为验证OxyR与上述预测的靶DNA的结合,分别进行了EMSA的验证分析。实验结果表明,OxyR与sgnM-sgnR启动子序列、RS24880启动子序列都能够特异性结合,突变结合位点GGTCC-15nt-CGGC-15nt-GCCG-9nt-GGACC中motif 1-4都能显著降低OxyR的结合能力,表明该保守序列是OyxR的特异性结合位点。
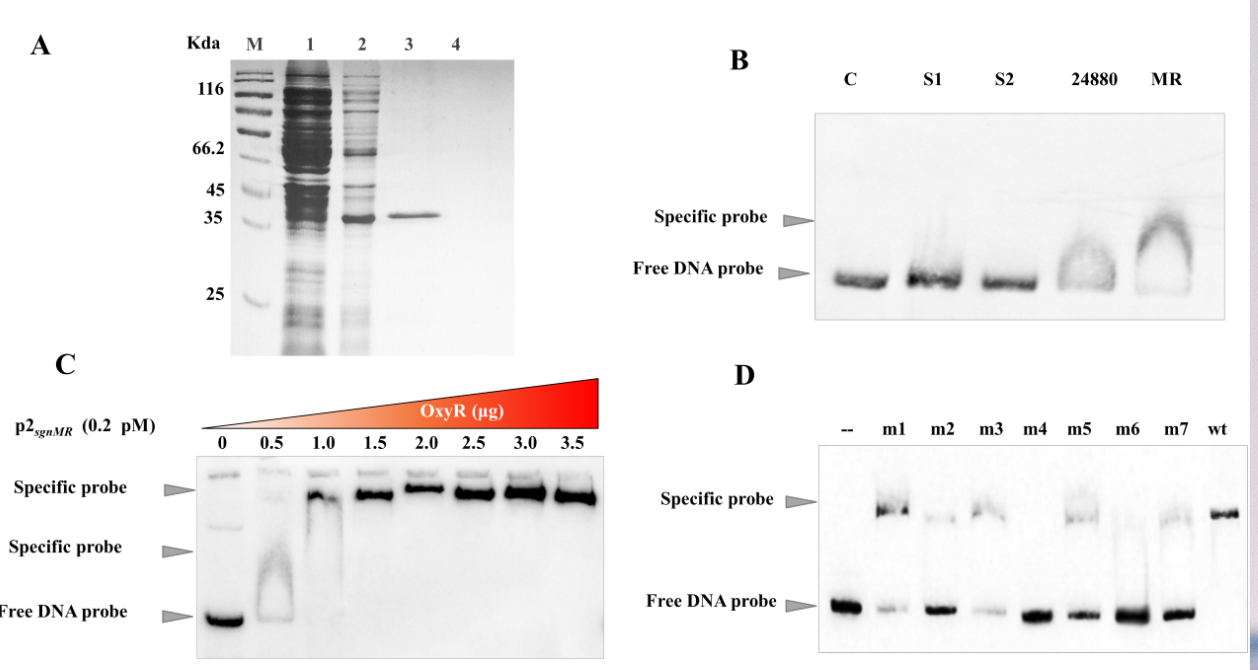
图7 OxyR与相关靶基因结合位点的EMSA验证
(A): OxyR-His 表达与纯化. M: maker; 1: 全菌蛋白; 2: pET-15b空载对照; 3: OxyR-His纯化蛋白;4 SDS-PAGE loading buffer. (B): oxyR与psgnMR 的EMSA b实验. (C): 竞争实验。(D) OxyR 结合位点突变对结合能力影响.
Western-blot分析发现,OxyR在纳他霉素生物合成和菌丝分化过程中,蛋白表达量变化不大(图8A),表明该蛋白调控纳他霉素生物合成和菌丝分化过程中,其调控作用的发挥可能不依赖表达量的变化。分析OxyR的ROS响应特点,其调控作用的变化可能通过其氧化还原状态的改变得以实现。通过进一步的氧化还原实验表明,OxyR在不同的ROS浓度下,可能表现出3种氧化还原状态(氧化态ox,还原态red,过氧化态pox)(图8 C、D),与前期在Vibrio vulnificus发现结果一致。

图8 OxyR 氧化及还原实验
(A) Western-blot分析OxyR的表达量. (B) 还原、氧化和过氧化OxyR 状态分析 .(C) 还原、氧化和过氧化OxyR 与 sgnMR 启动子探针的结合能力;C: control.1-4: 氧化态 OxyR 用1000 μM, 100 μM, 50 μM, 10 μM DTT处理; 5: 氧化态 OxyR; 6-10: 氧化态OxyR 用10 μM, 50 μM, 100 μM, 500μM, 1000 μM H2O2处理.
7. 基于ROS与纳他霉素生物合成关系构建纳他霉素高产工程菌
综合上述研究,SgnE催化麦角甾醇(Ergosterol)和豆甾醇(Stigmasterol)于胞外生成的H2O2对胞内H2O2浓度具有显著影响,且胞内H2O2可能作为信号分子与OxyR调控蛋白形成信号通路,通过途径特异性调控基因和RS24880基因转录的调控,对还原性次级代谢产物--纳他霉素生物的合成和菌丝分化具有调控作用。因此,H2O2对纳他霉素生物合成调控具有“浓度阈值激活效应”及纳他霉素对S. gilvosporeus生长的“H2O2稳态负反馈效应”:H2O2积累到阈值时,纳他霉素作为还原剂,其生物合成基因簇被激活并迅速表达合成纳他霉素,作为维持S. gilvosporeus内H2O2稳态的重要补充途径,负反馈清除胞内及胞外H2O2及胞外,动态调控H2O2稳态。因此,本课题依此理论,采用了大环内酯类抗生素高效外排泵基因adeABC,构建高效纳他霉素外排菌株,摇瓶发酵实验表明纳他霉素发酵产量提高约28%,且纳他霉素生物合成启动时间提前,至16h左右(图9)。
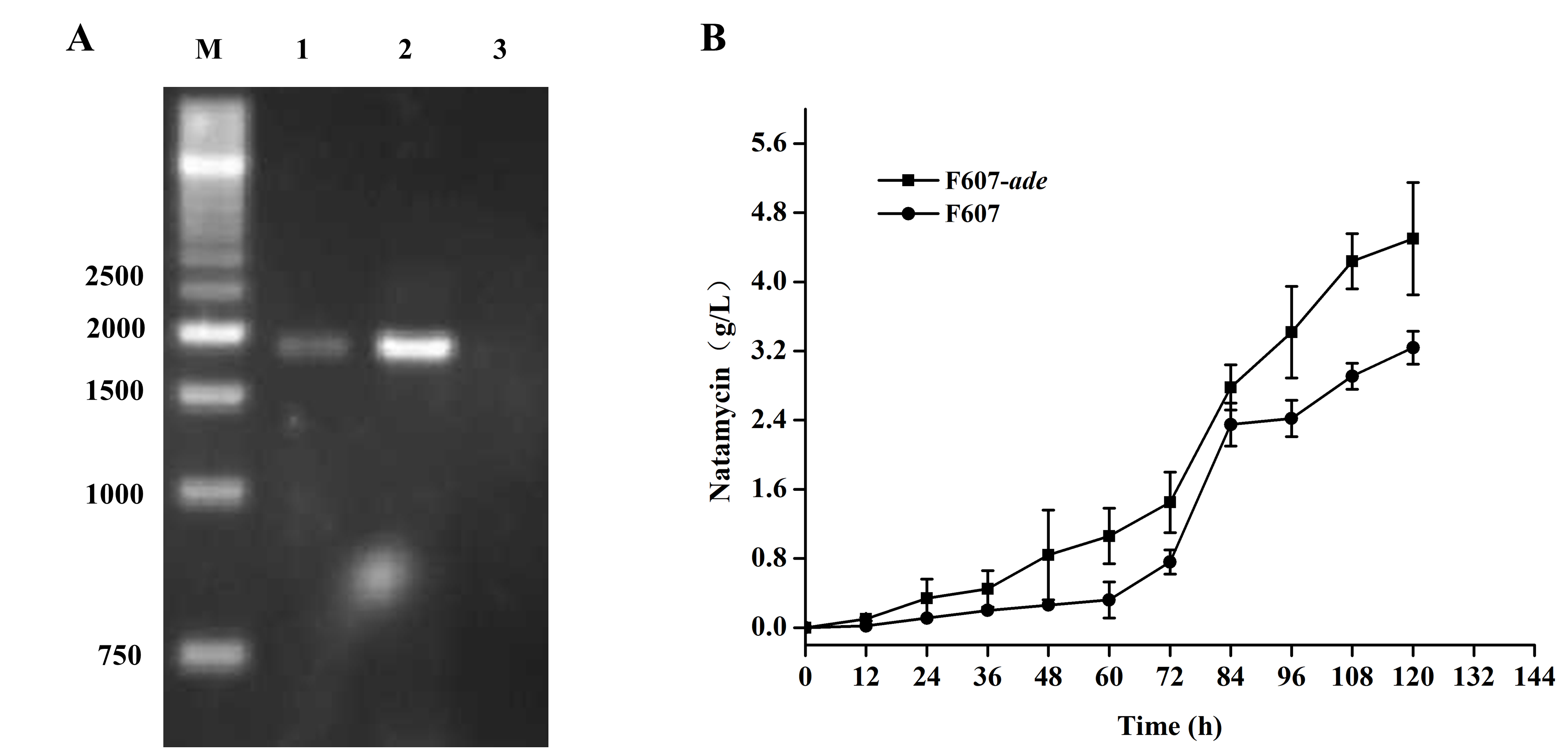
图9 纳他霉素高效外排菌株构建
(A) 纳他霉素高效外排菌株构建的PCR验证.M:maker;1:高效外排菌株;2:pMS-adeABC重组质粒对照;3:F607菌株对照。 (B) 纳他霉素高效外排菌株纳他霉素产量测定
(三)研究成果
本项目旨在证实“ROS-OxyR信号通路MI-MII分化过渡期激活纳他霉素的合成”的科学假说,通过本项目的研究。
(1)本项目创新性:传统理论认为次级代谢产物对该生物无明显生理功能,或并非是该生物生长和繁殖所必需的物质。本项目从氧化胁迫和纳他霉素合成和菌丝分化关系的视角,主要解决氧化胁迫分子开关OxyR别构调控途径特异性基因表达的分子机制这一关键科学问题。本项目的实施将证实OxyR是在MI-MII菌丝分化期,纳他霉素生物合成和氧化胁迫以及PCD交互作用的节点,是S. gilvosporeus中激活纳他霉素合成并抵御胞内H2O2损伤的一环,对菌体生长及适应环境氧化胁迫具有重要意义。
(2)达到了以下目标:
① 明确了MI-MII菌丝分化过渡期与纳他霉素合成的关系,阐明了ROS信号分子对激活纳他霉素生物合成的浓度阈值。
② 解析了褐黄孢链霉菌中OxyR氧化机制。体外及体内试验分别证实ROS对OxyRred的氧化激活作用、褐黄孢链霉菌对OxyRox的还原作用机制,解析了OxyR激活纳他霉素合成的靶基因及机制。
③ 针对H2O2对纳他霉素生物合成调控具有“浓度阈值激活效应”及纳他霉素对S. gilvosporeus生长的“H2O2稳态负反馈效应”,构建了纳他霉素高效外排菌株,提升纳他霉素的发酵产量28%,现已保存至广东微生物菌株保藏中心(NO.62228)。为构建纳他霉素高产菌株提供了新的思路,研究结果将为微生物菌株育种探索一种新途径。
(四)研究心得作全面总结
本项目将首次解析氧化胁迫与纳他霉素合成交互作用的调控机理,并填补纳他霉素合成的生理学意义上的空白,重新认识次级代谢产物对细菌生长和代谢的价值。对目前制约纳他霉素工业生产的瓶颈,高产基因工程菌株改造具有重要价值。本项目实施后,构建的菌株产量高,生产出成本低的纳他霉素将会有更强的市场竞争力。
二、项目创新点与特色:
(1)揭示 MI- MII 分化过渡期激活纳他霉素合成的信号分子是 ROS。MI- MII 分化过渡期是链霉菌中抗生素产生所必需的,但其调控作用途径是至今未解决的难题,本项目发现 MII 分化过程中产生大量的 ROS,可能是激活纳他霉素生物合成的信号分子。将有利于丰富对链霉菌发育、纳他霉素及链霉菌次级代谢调控机制的认识。
(2)分析菌丝分化进程与次级代谢激活之间的关键蛋白分子 OxyR,并将首次阐明接收 ROS 信号的结构域及其对纳他霉素生物合成的影响。与已报道的 OxyR 主要参与氧化应激反应及通过下游调控蛋白间接调控次级代谢及抗生素的方式不同,本项目提出 OxyR 响应 ROS 信号,形成信号通路,直接结合抗生素的途径特异性调控基因 sgnM或 sgnR 的表达,激活纳他霉素的生物合成。该调控途径的解析将进一步完善纳他霉素生物合成的调控网络和 OxyR 在次级代谢调控中作用的研究,并将揭示 OxyR 作为分子开关的作用机制。
(3)阐释 MI- MII 分化过渡期与纳他霉素生物合成之间“ ROS- OxyR- sgnM/R” 信号通路。在链霉菌研究领域,液体培养条件下,菌丝生长发育与次级代谢产物合成之间的关系一直是困扰该研究领域的一大难题。本研究首次阐释了 MI- MII 分化
过渡期与次级代谢产物之间的“ ROS- OxyR- sgnM/R” 信号通路。不仅将明确菌丝分化与次级代谢产物合成之间的 ROS 信号分子,还同时阐明 OxyR 作为调控蛋白激活纳他霉素生物合成的机制。将填补链霉菌生长发育过程中信号分子和抗生素
合成调控方面研究的空白,为解决菌丝生长发育与次级代谢产物合成之间的关系这一大难题提供了新的理论依据。
(4)为工业化高产量发酵抗生素提供了新的思路。孢子的产生会终止抗生素的生产,延后甚至抑制孢子的形成,尽可能的将链霉菌的发酵维持在抗生素大量产生的 MI- MII 分化过渡期提供了新的方向。